European Resuscitation Council, University of Antwerp, Bélgica
ArtículoAunque varios investigadores han observado que la incidencia de las paradas cardiacas está disminuyendo1, la supervivencia total continúa siendo decepcionantemente baja, de un 10% o inferior2. La enfermedad cardiovascular sigue siendo la causa del 41% del total de muertes en Europa. La parada cardiaca suele ser el primer síntoma catastrófico de un ataque de corazón.
Recientemente, varias organizaciones han intentado mejorar su cadena de supervivencia, de manera que se pueda reanimar hasta un 61% de las víctimas de paradas cardiacas que presentan fibrilación ventricular (FV) o taquicardia ventricular (TV)3, pero las revisiones sistemáticas muestran que los resultados difieren de forma muy notable en distintas regiones: las cifras de supervivencia publicadas oscilan entre el 6 y el 31% del total de paradas cardiacas, y entre el 8 y el 43% de las paradas con FV/TV4, 5, 6. Esta diferencia tan notable en la supervivencia es un reflejo de la denominada fórmula de supervivencia «ciencia + educación + implementación = supervivencia»7: la supervivencia a una parada cardiaca sólo podrá aumentarse mejorando nuestro conocimiento científico sobre el complejo de parada cardiaca-reanimación, perfeccionando la elaboración y la enseñanza de las guías basadas en la evidencia y optimizando la implementación de esas guías en todos los niveles de la práctica clínica de los cuidados cardiovasculares de emergencia (CCE).
PROCESO DE ELABORACIÓN DE LAS GUÍAS DE 2010 DEL EUROPEAN RESUSCITATION COUNCIL
La actualización de 2010 de las guías para la reanimación del European Resuscitation Council (ERC)8 se publicó el 10 de octubre de 2010 y se presentó formalmente en el 10th Scientific ERC Congress en diciembre de 2010 en Oporto, Portugal. En esta actualización de 2010 se continúa con la tradición de adaptar las guías en ciclos de 5 años.
Como en 2005, las guías de 2010 se basan en una revisión sistemática de los conocimientos científicos más recientes. El International Liaison Committee on Resuscitation (ILCOR), del que forman parte todos los consejos de reanimación de Europa, Estados Unidos, Canadá, Latinoamérica, Sudáfrica, Asia, Australia y Nueva Zelanda, se ha encargado de realizar este proceso de evaluación de la evidencia. Las conclusiones de esta revisión sistemática de la literatura se presentaron en la Consensus on Science Conference en febrero de 2010 en Dallas (Texas, Estados Unidos) y se publicaron con el título de «International Consensus on Cardiopulmonary Resuscitation Science and Treatment Recommendations» (CoSTR) el 10 de octubre de 2010, en las revistas Resuscitation y Circulation 9.
Este proceso ilustra el carácter dinámico del mecanismo de elaboración de las guías que utiliza la comunidad científica internacional dedicada a la reanimación: poco después de la publicación de las CoSTR de 2005 y de las guías de 2005, se hizo evidente que nuestro conocimiento científico sobre la reanimación es muy escaso y a menudo se basa en extrapolaciones, que la evidencia existente es poca y que las modificaciones deben ser impulsadas por argumentos tanto científicos como de formación.
El ILCOR identificó los principales campos en los que había una falta de conocimiento científico en la publicación de 2007 de Gazmuri et al10. Esta publicación sirvió de guía para iniciar nuevas investigaciones de interés y para estructurar la CoSTR de 2010 y el proceso de elaboración de las guías. Esta revisión de los datos científicos de la CoSTR de 2010 se llevó a cabo siguiendo una metodología estrictamente estandarizada. Un total de 313 expertos revisaron 277 temas. Cada revisión la realizó un equipo de al menos dos expertos de organizaciones distintas pertenecientes al ILCOR. Se aplicó una política de «conflictos de intereses» estricta para garantizar la máxima objetividad.
Después de cada modificación introducida en las guías, debe iniciarse un complejo mecanismo para difundir e implementar los cambios en la práctica clínica. Este es un esfuerzo importante, que tienen que llevar a cabo las organizaciones que forman parte del ILCOR, cada consejo de reanimación nacional y miles de instructores. Debemos tener en cuenta que son necesarios al menos 2 años para que las nuevas guías sean aplicadas en la práctica clínica de los servicios de emergencias médicas (SEM).
En consecuencia, en el proceso de elaboración de las guías de 2010 se aplicó el principio de que no se introduce ningún cambio a no ser que haya nuevas evidencias suficientes y que la sencillez es crucial para una aceptación amplia en todo el mundo.
Desde un punto de vista científico, un proceso de actualización continuo, con publicaciones regulares de artículos de posicionamiento a medida que aparecen nuevos datos científicos podría ser una opción razonable. Sin embargo, en aras de conseguir mejores aceptación, enseñanza e implementación, se consideró importante elaborar una actuación por plazos, de manera que pudiera constituir una referencia para todos los involucrados en la reanimación. Así pues, se mantiene el ciclo de 5 años.
GUÍAS DE 2010 PARA LA REANIMACIÓN CARDIOPULMONAR EN LA PARADA CARDIACA EXTRAHOSPITALARIA DE ADULTOS: ¿QUÉ HA CAMBIADO Y POR QUÉ?
En todos los aspectos de las guías de 2010 se resalta la importancia de realizar unas compresiones torácicas de buena calidad e ininterrumpidas. Las compresiones torácicas de buena calidad se aplican a una frecuencia de al menos 100 por minuto, con una profundidad de compresión de al menos 5cm, y se interrumpen lo menos posible para realizar otras maniobras como la desfibrilación, el mantenimiento de las vías aéreas y la administración de fármacos.
Las diferencias basadas en la evidencia más relevantes respecto a las guías de 2005 para el soporte vital básico (SVB) y el soporte vital avanzado (SVA) en adultos con parada cardiaca son las siguientes8:
Cambios en el soporte vital básico en las guías de 2010 12
• Identificación precoz centrada en la falta de respuesta y en la calidad de la respiración. Se resalta la importancia del boqueo como signo de parada cardiaca.
• Todos los reanimadores, con o sin formación, deben realizar compresiones torácicas a las víctimas de una parada cardiaca. La aplicación de compresiones torácicas de alta calidad es esencial. El objetivo debe ser empujar hasta una profundidad de al menos 5 cm y a una frecuencia de al menos 100 compresiones por minuto, permitir una recuperación plena de la posición del tórax y reducir al mínimo las interrupciones de las compresiones torácicas. Los reanimadores con formación deben aplicar también ventilaciones, con una proporción de compresión-ventilación de 30:2. Se recomienda una reanimación cardiopulmonar (RCP) con compresión torácica sola, guiada por teléfono, para los reanimadores sin formación.
Cambios en las estrategias de desfibrilación en las guías de 2010 13
• Reducir al mínimo la duración de las pausas previa y posterior a la descarga; continuar con las compresiones durante la carga del desfibrilador y reanudarlas inmediatamente después de la desfibrilación; la aplicación de la desfibrilación debe poder hacerse con una interrupción de las compresiones torácicas no superior a 5 s.
• Se ha dejado de recomendar la aplicación sistemática de un periodo preespecificado de RCP (p. ej., 2 o 3 min) antes de un análisis del ritmo y la descarga.
• Se recomienda continuar desarrollando los programas de desfibrilador externo automático (DEA) y es necesario desplegar más ampliamente los DEA tanto en lugares públicos como en áreas residenciales.
Cambios en las guías de 2010 para el soporte vital avanzado 14
• Importancia de las compresiones torácicas de alta calidad, con interrupciones mínimas, en cualquier intervención de SVA: se realizan pausas breves en las compresiones torácicas únicamente para permitir la aplicación de intervenciones específicas.
• Ha dejado de resaltarse el papel del golpe precordial.
• Si no puede obtenerse una vía intravenosa, los fármacos deben administrarse por vía intraósea y no a través de un tubo traqueal.
• Al tratar un parada cardiaca con FV/TV, se administra adrenalina 1mg después de la tercera descarga y luego cada 3-5 min. Se administra también amiodarona 300 mg después de la tercera descarga.
• Ha dejado de recomendarse el uso sistemático de atropina en la asistolia o la actividad eléctrica sin pulso.
• La intubación traqueal temprana sólo se recomienda si la practican reanimadores muy capacitados que puedan aplicarla con una interrupción mínima de las compresiones torácicas.
• Se hace mayor énfasis en el uso de capnografía y en el posible efecto nocivo de la hiperoxemia tras la recuperación de la circulación espontánea (RECE): el oxígeno inspirado debe ajustarse a una saturación arterial de oxígeno del 94-98% (o el 88-92% si el paciente tiene riesgo de insuficiencia respiratoria hipercápnica).
• Un protocolo de tratamiento tras la reanimación completo y estructurado incluye intervención coronaria percutánea (ICP), control de la glucemia y de las crisis epilépticas e hipotermia terapéutica.
Estos cambios están respaldados por una evidencia científica de buena calidad y son importantes para mejorar las probabilidades de supervivencia. Así pues, los cambios se basan en nuevas evidencias científicas disponibles y en la necesidad de simplificación para la enseñanza.
El algoritmo universal de 2010 ilustra los cambios introducidos en la RCP por acuerdo de todas las organizaciones que forman parte del ILCOR (figura 1).
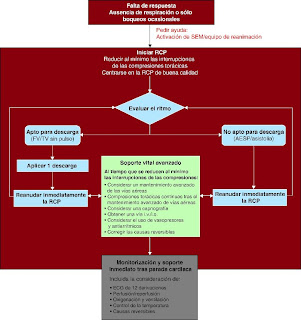
Figura 1. Algoritmo universal de reanimación de ILCOR 2010 9 (reproducido con permiso del ILCOR). AESP: actividad eléctrica sin pulso; ECG: electrocardiograma; FV: fibrilación ventricular; i.o.: intraóseo; i.v.: intravenoso; ILCOR: International Liaison Committee on Resuscitation; RCP: reanimación cardiopulmonar; SEM: servicios de emergencias médicas; TV: taquicardia ventricular.
Podríamos hacer la siguiente reflexión: «si el conocimiento científico es el mismo, ¿por qué no enseñamos lo mismo?». Sabemos que la evidencia científica guía la práctica y que hay un ajuste fino basado en la experiencia personal y que está en relación con el paciente, el sistema de asistencia y las características demográficas. En consecuencia, partiendo de un conocimiento científico común, cada una de las principales organizaciones que forman parte del ILCOR adaptó sus propias guías de práctica clínica de manera que reflejaran las diferencias existentes en cuanto a organización, legislación, disponibilidad de fármacos y dispositivos, prioridades, características demográficas y características de los pacientes y los reanimadores15.
HACIA 2015: ¿QUÉ LAGUNAS HAY EN NUESTRO CONOCIMIENTO?
Al igual que ocurrió en 2005, durante la redacción de las guías de 2010 se puso ya de manifiesto que nuestro conocimiento del complejo de parada cardiaca-reanimación continúa siendo muy fragmentario. Los avances en cuanto a la supervivencia tras la parada cardiaca continuarán siendo pequeños mientras en nuestro conocimiento siga habiendo lagunas importantes pendientes de aclarar.
El progreso de los conocimientos científicos es alentador, pero continúa siendo demasiado lento. Esto se pone de relieve en la sorprendente observación realizada por Ornato et al de que el National Heart, Lung, and Blood Institute financió en el periodo 1985-2009 un total de 6.886 estudios en el campo del infarto agudo de miocardio, 4.403 en el del ictus, 9.919 en el de la insuficiencia cardiaca y sólo 257 en el de la parada cardiaca y la reanimación16. Esto contrasta claramente con el hecho conocido de que cada año fallecen en Estados Unidos 157.000 personas por infarto agudo, 150.000 por ictus y 284.000 por insuficiencia cardiaca, frente a 310.000 por parada cardiaca. Ello hace que no sólo sea necesario un cambio en la política de los organismos y las organizaciones responsables de la financiación de la investigación traslacional, sino también un interés y una motivación mucho mayores para realizar estudios de buena calidad por los investigadores que forman parte de las organizaciones afiliadas al ILCOR.
Las lagunas importantes de nuestro conocimiento tras las guías de 2010 para el manejo de la parada cardiaca en adultos mediante SVB y SVA incluyen lo siguiente:
• ¿Cómo puede optimizarse la identificación precoz de la parada cardiaca?
• ¿Cuál es la estrategia óptima para la prevención de la parada cardiaca, en el hospital y fuera de él?
• ¿Cuáles son la frecuencia y la profundidad óptimas de las compresiones torácicas?
• ¿Qué efectividad tiene la ventilación efectuada por testigos presenciales?
• ¿Cuál es la estrategia óptima para el acceso rápido al paciente en parada cardiaca en su domicilio?
• ¿Cuál es el mejor momento para aplicar la compresión torácica tras la desfibrilación?
• ¿Qué efecto tiene la compresión sola en la supervivencia y la disposición a aplicar una RCP?
• ¿Qué efecto tienen los dispositivos de compresión torácica automáticos en los resultados?
• ¿Cuándo y cómo deben utilizarse las mascarillas con válvula y balón (ambú) y cuándo es mejor aplicar técnicas avanzadas de mantenimiento de las vías aéreas?
• ¿Cuál es el mejor método para confirmar la colocación correcta de un tubo traqueal?
• ¿Cuánto oxígeno es necesario en función de las condiciones clínicas, y cómo debe administrarse?
• ¿Cuáles son la frecuencia de ventilación y el volumen corriente óptimos?
• ¿Cuál es el papel de la estimulación con marcapasos en la RCP?
• ¿Qué efectividad tienen los fármacos (analgésicos, sedantes, atropina, amiodarona, vasopresores, tampones, calcio, antitrombóticos, antiagregantes plaquetarios, líquidos, etc.) en cuanto a la supervivencia en diferentes condiciones clínicas?
• ¿Existen variables sencillas y fiables que sean útiles para el pronóstico y la decisión de iniciar/interrumpir el tratamiento?
• ¿Qué papel debe desempeñar la ICP tras la RECE y cómo debemos tratar la parada cardiaca durante una ICP y tras la cirugía cardiaca?
• ¿Cuál es la estrategia óptima para la reperfusión temprana en los síndromes coronarios agudos?
• ¿Cuál es la temperatura, el momento de aplicación, el método y la rapidez de aplicación óptimos de la hipotermia terapéutica, durante y después de la parada cardiaca?
• ¿Cómo debemos ajustar los protocolos de donación de órganos a las nuevas estrategias de tratamiento (incluida la hipotermia terapéutica)?
BÚSQUEDA DE LA CALIDAD: DEBEMOS HACERLO MEJOR; TENEMOS QUE SABER MÁS
Cualquier tipo de gestión de la calidad en medicina, como en la industria, se basa en el paradigma de que tenemos que conocer nuestra situación actual y los objetivos finales para poder planificar la forma de alcanzarlos.
Así pues, es esencial disponer de datos basales: datos basales fiables respecto a la epidemiología de la parada cardiaca, respecto al proceso de la parada cardiaca y la reanimación, respecto a los resultados. Y eso es exactamente lo que nos falta. No sólo en Europa, sino en todo el mundo.
La comunidad internacional involucrada en la reanimación, a través del ILCOR, ha elaborado la terminología Utstein, un lenguaje común y un conjunto de definiciones para describir el complejo de la parada cardiaca-reanimación. Este lenguaje uniforme es esencial para comprender la naturaleza de los resultados presentados y para comparar datos de diferentes orígenes. La terminología Utstein se desarrolló en 1991 para la parada cardiaca extrahospitalaria y hospitalaria17, 18 y se actualizó en 200419. Actualmente, 7 años y 2 guías después, podría ser apropiado considerar una nueva actualización del patrón original y su adaptación a la práctica clínica moderna y a las guías que incluyen características diferentes de las víctimas de parada cardiaca en lugares privados y públicos, un SVB simplificado y DEA aplicados por reanimadores sin formación, nuevos protocolos de SVA, nuevos conocimientos sobre fármacos y dispositivos, la hipotermia terapéutica, la ICP, etcétera.
Y debemos recordar siempre que los datos presentados deben interpretarse en el contexto de los criterios de inclusión y exclusión:
• ¿Se incluyen todos los episodios de parada cardiaca? ¿Solamente las paradas cardiacas atendidas por miembros del SEM? ¿Sólo las de presunto origen cardiaco? Adultos y niños, ¿fuera del hospital, en el domicilio, en el hospital?
• ¿Hay pacientes en los que no se plantee la reanimación y por qué?
• ¿Hay datos de centros de notificación voluntaria o de informes sistemáticos en toda la región/país?
En consecuencia, hay algunas preguntas sencillas que por el momento continúan sin respuesta:
• ¿Qué incidencia tiene la parada cardiaca en Europa?
• ¿Cuál es la evolución tras la parada cardiaca en Europa?
• ¿Cómo podemos aprender de la práctica utilizada en las regiones que obtienen los mejores resultados para mejorar nuestra cadena de supervivencia local concreta?
Europa podría definirse según hace el Consejo de Europa20 e incluye 47 países con una población total de 830 millones de habitantes. El ERC ha decidido adoptar esta definición, que es algo diferente para otras definiciones regionales y políticas. Esto es de la máxima importancia, puesto que sabemos que cada uno de estos 47 países tiene sus propias características demográficas, prioridades sanitarias, organización, sistema de asistencia, legislación y tradición.
Varios investigadores han intentado estimar la incidencia de la parada cardiaca en Europa y también en Norteamérica. Estos estudios son muy instructivos, pero tienen en común la misma limitación de que presentan datos de centros seleccionados y muy motivados, lo que puede no reflejar la práctica clínica real. Se han publicado algunos artículos clave, como el de Sans et al21, que examinaron los datos de mortalidad de 30 países europeos, el de Herlitz et al22, que compararon los datos de 38 sistemas de SEM europeos, el de Atwood et al23, que obtuvieron datos de 37 centros europeos en 1980-2004, y el de Berdowski et al6, que analizaron los informes de 30 centros de SEM europeos en 1986-2009. Se han publicado otros muchos estudios en el contexto de cuestiones específicas (como el de Böttiger et al24 sobre los fibrinolíticos en la parada cardiaca, las Euro Heart Survey sobre el uso de la ICP25, 26 y los informes de estadísticas cardiovasculares de la Comisión Europea27).
Estos estudios tienen también limitaciones, por cuanto incluyen solamente partes de Europa, durante un largo periodo, con datos que pueden tener un sesgo de notificación, incluyen solamente paradas cardiacas atendidas por miembros del SEM, con información limitada acerca de los episodios intrahospitalarios y domiciliarios y, por último, aportan poca información acerca de la secuencia completa de «entrada-proceso-salida» o «paciente-intervención-resultado».
De forma similar, en Norteamérica, están en funcionamiento varios registros multicéntricos, con los mismos objetivos de vigilancia, análisis y mejora de los eslabones sucesivos de la cadena de la parada cardiaca y la reanimación. Tres registros de centros de alta calidad, el Resuscitation Outcomes Consortium (ROC) Epistry Cardiac Arrest28, el Cardiac Arrest Registry to Enhance Survival (CARES)29 y el American Heart Association's National Registry of CardioPulmonary Resuscitation (NRCPR)30, cuentan con la ventaja de un sistema de SEM estandarizado y una legislación uniforme que permite realizar comparaciones válidas entre los centros.
La situación de Europa es radicalmente diferente de la de Norteamérica: cada país tiene sus propios sistemas de SEM, con legislaciones y tipos diferentes, el SEM está organizado en forma de un sistema de uno o dos niveles y el SVA puede ser realizado por personal paramédico, enfermeras o médicos; todo ello hace que un registro unificado en Europa sea mucho más complejo.
En consecuencia, nuestra mejor aproximación es que en Europa hay una incidencia de parada cardiaca por todas las causas de 0,4-0,9/1.000/año, con una supervivencia que oscila entre el 6 y el 31%. Para las paradas cardiacas que cursan con FV/TV, estimamos que la incidencia es de 0,2/1.000/año, con una supervivencia que oscila entre el 8 y el 43%.
Las razones que explican estas diferencias observadas en la supervivencia no están claras: ¿se trata de hechos o de artefactos? En esta población de 830 millones en 47 países, con la gran variabilidad de características demográficas, legislaciones y sistemas de asistencia, las diferencias observadas pueden ser el resultado de diferencias en las definiciones, en los criterios de inclusión, en los sistemas de obtención de datos o en la calidad de los datos o puede tratarse de diferencias reales.
En 2008, el ERC creó un grupo de trabajo con el objetivo de establecer un European Registry of Cardiac Arrests (EuReCa) uniforme, basado en las experiencias existentes de los países miembros y en las definiciones uniformes de la terminología Utstein. Debe englobar las diferencias existentes en estructura, organización e intervenciones del SEM, al tiempo que incluye la intervención de participantes diversos, como testigos presenciales, personal de ambulancia y especialistas en cuidados críticos.
La obtención del conjunto de datos clave Utstein completos puede plantear dificultades, y este objetivo puede resultar difícil de alcanzar para las organizaciones de SEM. Sin embargo, esto no debe desalentar a los sistemas de SEM respecto al seguimiento de sus resultados. Debemos tener presente que son necesarias diferentes partes de los datos clave Utstein para poder conocer la epidemiología de la parada cardiaca, el proceso de reanimación y el resultado final. Los sistemas de SEM pueden optar inicialmente por el registro de partes específicas del conjunto de datos, aunque no sean todas.
El objetivo principal del ERC es mejorar la calidad y los resultados de la reanimación aplicada a las personas que sufren una parada cardiaca en Europa. El EuReCa puede facilitar este objetivo, ya que permitirá:
• Estandarización de las definiciones, de manera que puedan aplicarse de modo más uniforme.
• Comparación válida del proceso y el resultado en diferentes regiones y países.
• Identificación de los puntos débiles en los eslabones locales, regionales o nacionales de la cadena de la supervivencia, y una ayuda para la mejora.
• Seguimiento de la implementación y el efecto de las nuevas guías.
• Creación de una red de cooperación científica nacional e internacional en el campo de la RCP.
Como primera actividad del EuReCa, se recogieron datos de paradas cardiacas tratadas en 2008 por el SEM en 5 áreas diferentes de Bélgica, Alemania, Países Bajos, Suecia y España que engloban a una población de 34,9 millones de personas y notificaron 12.446 intentos de reanimación en 1 año. La incidencia de paradas cardiacas presentó diferencias entre las distintas regiones, entre 17 y 53/100.000 habitantes/año, y la tasa de ingresos en el hospital fue de entre 5 y 18/100.000 habitantes/año.
La primera obtención de datos pone de relieve las limitaciones y los obstáculos que tiene esta recogida de información de ámbito nacional, incluidos los obstáculos legales para la comunicación de datos acerca del escenario prehospitalario y hospitalario y acerca de la supervivencia. El proyecto confirmó también la diferencia previamente observada de 3 veces en la incidencia, la participación de testigos presenciales, el uso de DEA y la supervivencia: ¿hechos o artefactos?
En resumen, todas las organizaciones de reanimación europeas y las autoridades nacionales y europeas comparten la responsabilidad de realizar un seguimiento de la enorme carga que supone la parada cardiaca para la sociedad, de implementar las actuales guías basadas en la evidencia y de informar sobre el proceso de reanimación y sus resultados y mejorarlo en sus regiones. Esto sólo es posible con el registro de las variables clave y el uso de un estilo de notificación uniforme que permite la identificación y la valoración de las consecuencias de las diferencias existentes en los sistemas de asistencia que se utilizan dentro de Europa. En la Unión Europea, actualmente hay una apreciación creciente de las repercusiones que tienen las paradas cardiacas, de la necesidad de acceder a unos datos fiables sobre ellas y sus resultados, de manera que pueda establecerse en Europa una política dinámica para la implementación de un tratamiento óptimo de la parada cardiaca.
Conflicto de intereses
Ninguno.
Full English text available from: www.revespcardiol.org
Autor para correspondencia: University of Antwerp, Faculty of Medicine, Universiteitsplein, 1, BE2610 Antwerp, Bélgica. leo.bossaert@ua.ac.be
Bibliografía1.Cobb L, Fahrenbruch C, Olsufka M, Copass M. Changing incidence of out of hospital ventricular fibrillation 1980-2000. JAMA. 2002; 288:3008-13.
Pubmed 2.Nichol G, Stiell I, Laupacis A, Pham B, De Maio V, Wells G. A cumulative meta-analysis of the effectiveness of defibrillator-capable emergency medical services for victims of out-of-hospital cardiac arrest. Ann Emerg Med. 1999; 34:517-25.
Pubmed 3.Sunde K, Pytte M, Jacobsen D, Mangschau A, Jensen LP, Smedsrud C, et-al. Implementation of a standardised treatment protocol for post resuscitation care after out-of-hospital cardiac arrest. Resuscitation. 2007; 73:29-39.
Pubmed 4.Nichol G, Thomas E, Callaway CW, Hedges J, Powell JL, Aufderheide TP, et-al. Regional variation in out-of-hospital cardiac arrest incidence and outcome. JAMA. 2008; 300:1423-31.
Pubmed 5.Nichol G, Aufderheide TP, Eigel B, Neumar RW, Lurie KG, Bufalino VJ, et-al. Regional systems of care for out-of-hospital cardiac arrest: A policy statement from the American Heart Association. Circulation. 2010; 121:709-29.
Pubmed 6.Berdowski J, Berg R, Tijssen J, Koster R. Global incidences of out-of-hospital cardiac arrest and survival rates: Systematic review of 67 prospective studies. Resuscitation. 2010; 81:1479-87.
Pubmed 7.Chamberlain DA, Hazinski MF. European Resuscitation Council, American Heart Association, Heart and Stroke Foundation of Canada. Australia and New Zealand Resuscitation Council, et al. Education in resuscitation. Resuscitation. 2003; 59:11-43.
Pubmed 8.Nolan J, Soar J, Zideman D, Biarent D, Bossaert L, Deakin C, et-al. European Resuscitation Council Guidelines for Resuscitation 2010 Section 1. Executive summary. Resuscitation. 2010; 81:1219-76.
Pubmed 9.Nolan JP, Hazinski MF, Billi JE, Boettiger BW, Bossaert L, De Caen AR, et-al. Part 1: Executive summary: 2010 International Consensus on Cardiopulmonary Resuscitation and Emergency Cardiovascular Care Science With Treatment Recommendations. Resuscitation. 2010; 81(Suppl 1):e1-25.
Pubmed 10.Gazmuri R, Nolan J, Nadkarni V, Arntz HR, Billi JE, Bossaert L, et-al. Scientific knowledge gaps and clinical research priorities for cardiopulmonary resuscitation and emergency cardiovascular care identified during the 2005 International Consensus Conference on ECC and CPR Science with Treatment Recommendations. A consensus statement from the International Liaison Committee on Resuscitation; the American Heart Association Emergency Cardiovascular Care Committee; the Stroke Council; and the Cardiovascular Nursing Council. Resuscitation. 2007; 75:400-11.
Pubmed 11.Berdowski J, Schmohl A, Tijssen J, Koster R. Time needed for a regional emergency medical system to implement resuscitation Guidelines 2005 — The Netherlands experience. Resuscitation. 2009; 80:1336-41.
Pubmed 12.Koster R, Baubin M, Bossaert L, Caballero A, Cassan P, Castrén M, et-al. European Resuscitation Council Guidelines for Resuscitation 2010: Section 2. Adult basic life support and use of automated external defibrillators. Resuscitation. 2010; 81:1277-92.
Pubmed 13.Deakin C, Nolan J, Sunde K, Koster R. European Resuscitation Council Guidelines for Resuscitation 2010. Section 3: Electrical therapies: Automated external defibrillators, defibrillation, cardioversion and pacing. Resuscitation. 2010; 81:1293-304.
Pubmed 14.Deakin C, Nolan J, Soar J, Sunde K, Koster RW, Smith GB, et-al. European Resuscitation Council Guidelines for Resuscitation 2010: Section 4. Adult advanced life support. Resuscitation. 2010; 81:1305-52.
Pubmed 15.Field J, Hazinski MF, Sayre M, Chameides L, Schexnayder SM, Hemphill R, et-al. Part 1: executive summary: 2010 American Heart Association Guidelines for Cardiopulmonary Resuscitation and Emergency Cardiovascular Care. Circulation. 2010; 122:S640-56.
Pubmed 16.Ornato J, Becker L, Weisfeldt M, Wright B. Cardiac arrest and resuscitation: an opportunity to align research prioritization and public health need. Circulation. 2010; 122:1876-9.
Pubmed 17.Cummins R, Chamberlain D, Abramson N, Allen M, Baskett PJ, Becker L, et-al. Recommended guidelines for uniform reporting of data from out-of-hospital cardiac arrest: the Utstein Style. A statement for health professionals from a task force of the American Heart Association, the European Resuscitation Council, the Heart and Stroke Foundation of Canada, and the Australian Resuscitation Council. Circulation. 1991; 84:960-75.
Pubmed 18.Cummins R, Chamberlain D, Hazinski MF, Nadkarni V, Kloeck W, Kramer E, et-al. Recommended guidelines for reviewing, reporting, and conducting research on in-hospital resuscitation: the in-hospital ‘Utstein style’. A statement for healthcare professionals from the American Heart Association, the European Resuscitation Council, the Heart and Stroke Foundation of Canada, the Australian Resuscitation Council, and the Resuscitation Councils of Southern Africa. Resuscitation. 1997; 34:151-83.
Pubmed 19.Jacobs I, Nadkarni V, Bahr J, Berg RA, Billi JE, Bossaert L, et-al. Cardiac arrest and cardiopulmonary resuscitation outcome reports: update and simplification of the Utstein templates for resuscitation registries. A statement for healthcare professionals from a task force of the international liaison committee on resuscitation (American Heart Association, European Resuscitation Council, Australian Resuscitation Council, New Zealand Resuscitation Council, Heart and Stroke Foundation of Canada, InterAmerican Heart Foundation, Resuscitation Council of Southern Africa). Resuscitation. 2004; 63:233-49.
Pubmed 20. Council of Europe [citado 15/2/2011]. Disponible en: www.coe.int.
21.Sans S, Kesteloot H, Kromhout D. The burden of cardiovascular diseases mortality in Europe. Eur Heart J. 1997; 18:1231-48.
Pubmed 22.Herlitz J, Bahr J, Fischer M, Kuisma M, Lexow K, Thorgeirsson G. Resuscitation in Europe: a tale of five European regions. Resuscitation. 1999; 41:121-31.
Pubmed 23.Atwood C, Eisenberg M, Herlitz J, Rea T. Incidence of EMS-treated out-of-hospital cardiac arrest in Europe. Resuscitation. 2005; 67:75-80.
Pubmed 24.Böttiger B, Bode C, Kern S, Gries A, Gust R, Glätzer R, et-al. Efficacy and safety of thrombolytic therapy during initially unsuccessful cardiopulmonary resuscitation. Lancet. 2001; 357:1583-5.
Pubmed 25.Widimsky P, Wijns W, Fajadet J, De Belder M, Knot J, Aaberge L, et-al. Reperfusion therapy for ST elevation acute myocardial infarction in Europe: description of the current situation in 30 countries. Eur Heart J. 2010; 31:943-57.
Pubmed 26.Müller-Nordhorn J, Binting S, Roll S, Willich S. An update on regional variation in cardiovascular mortality within Europe. Eur Heart J. 2008; 29:1316-26.
Pubmed 27. Health at a Glance: Europe 2010. OECD; 2010 [citado 15/2/2011]. Disponible en: http://dx.doi.org/10.1787/health_glance-2010-en.
28.Hostler D, Thomas E, Emerson S, Christenson J, Stiell IG, Rittenberger JC, et-al. Increased survival after EMS witnessed cardiac arrest. Observations from the Resuscitation Outcomes Consortium (ROC) Epistry-Cardiac arrest. Resuscitation. 2010; 81:826-30.
Pubmed 29.McNally B, Stokes A, Crouch A, Kellermann A. CARES: Cardiac Arrest Registry to Enhance Survival. Ann Emerg Med. 2009; 54:674-83.
Pubmed 30.Nadkarni V, Larkin L, Peberdy M, Carey SM, Kaye W, Mancini ME, et-al, for the National Registry of Cardiopulmonary Investigators. First documented rhythm and clinical outcome from in-hospital cardiac arrest among children and adults. JAMA. 2006; 295:50-7.

No hay comentarios:
Publicar un comentario